La FDA pone en la mira a las clínicas que venden ‘terapias’ con células madre no aprobadas
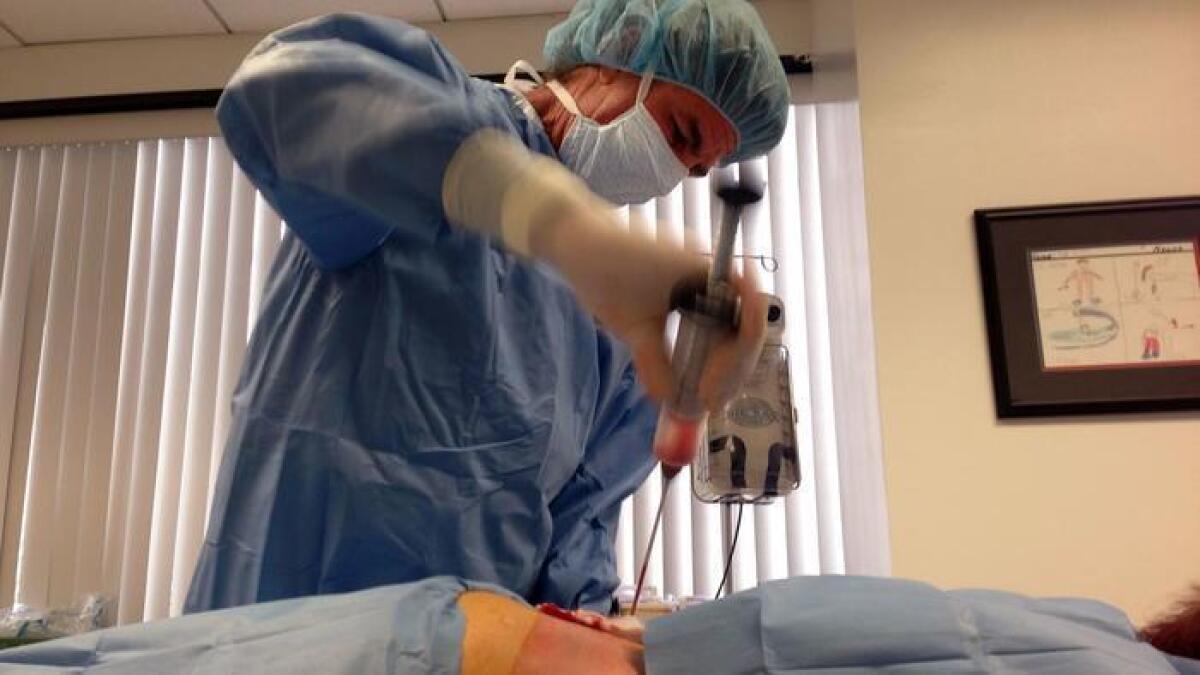
El Dr. Mark Berman toma grasa de la espalda de un paciente como parte de un procedimiento experimental con células madre, en una clínica de Beverly Hills. La Administración de Alimentos y Drogas endureció sus controles contra esos tratamientos no aprobados, que se realizan en clínicas de todo el país (Raquel Maria Dillon / AP).
La Administración de Alimentos y Drogas (FDA, por sus siglas en inglés) lanzó un ataque contra un mercado nacional en auge de tratamientos médicos sospechosos y anunció acciones que podrían frenar a las clínicas que ofrecen cuestionables procedimientos con células madre para enfermedades como el cáncer y otras.
Los blancos iniciales de la FDA fueron dos sucursales del California Stem Cell Treatment Centers, en Beverly Hills y Rancho Mirage; StemImmune Inc., de San Diego; y US Stem Cell Clinic de Sunrise, Florida.
Tomando una “acción decisiva” para proteger a los pacientes, la FDA envió el viernes último alguaciles federales a las clínicas de California y confiscó cerca de 500 dosis de vacunas contra la viruela, suministradas por StemImmune. La vacuna sería mezclada con células madre obtenida de la grasa de los pacientes y luego inyectada directamente en los tumores malignos de estos.
La FDA describió el procedimiento como “un tratamiento no aprobado y potencialmente peligroso contra el cáncer”, según un comunicado emitido este lunes. Uno de los cinco viales de las vacunas estaba abierto y “parcialmente utilizado”, destacó el organismo.
La incautación de la vacuna contra la viruela fue necesaria “para prevenir el uso de tratamientos potencialmente peligrosos y no aprobados”, según la agencia. Para los pacientes con cáncer -así como para las embarazadas o las personas inmunodeprimidas que entren en contacto con ellos- la exposición a la vacuna contra la viruela podría desencadenar una reacción potencialmente fatal: la inflamación o hinchazón del corazón y los tejidos circundantes.
La FDA afirmó que investigará cómo StemImmune Inc. obtuvo cinco viales de esta vacuna, que no está disponible en el mercado y que normalmente se reserva para quienes corren riesgo de exposición a esa enfermedad, como el personal militar y los trabajadores de la salud.
StemImmune no respondió a los llamados por parte de este periódico. En tanto, el Dr. Mark Berman, cofundador de los California Stem Cell Treatment Centers, fue desafiante en su declaración. Berman consideró los comentarios de la FDA y su comisionado, el Dr. Scott Gottleib, “despectivos y poco representativos”, y afirmó que mostraban “una falta de entendimiento” de los procedimientos quirúrgicos en los cuales las propias células madre de los pacientes se emplean para promover la regeneración. Berman, quien es también director de implantación de células madre en StemImmune, consideró que las ofertas de las clínicas son “una terapia de avanzada contra el cáncer” para pacientes en estadio cuatro.
También el lunes, la FDA emitió una carta de advertencia a la directora científica de la US Stem Cell Clinic, Kristin Comella, por la comercialización de productos con células madre sin la aprobación de la agencia. La misiva le dio a la clínica 15 días para explicar cómo abordará “estas significativas desviaciones” en sus prácticas de fabricación, que según la FDA ponen sus productos en riesgo de contaminación y a sus pacientes en peligro de infecciones.
Los productos de la clínica se administraban de forma intravenosa o directamente en la médula espinal de los pacientes, para tratar una variedad de enfermedades graves, entre ellas el Parkinson, la esclerosis lateral amiotrófica (o enfermedad de Lou Gehrig), enfisema, condiciones cardíacas y fibrosis pulmonar.
La FDA acusó a la US Stem Cell Clinic “de intentar impedir la investigación” de la agencia al negar la entrada de los agentes, excepto mediante una cita previa, y negándoles acceso a sus empleados. Ambas acciones violan la ley federal.
No se trata de la primera polémica de la clínica de Florida: en marzo pasado, un artículo publicado en el New England Journal of Medicine detalló los casos de tres pacientes con degeneración de la mácula, que quedaron ciegos poco después de recibir tratamientos con células madre para tratar esa enfermedad en dicho centro médico.
Al anunciar las dos acciones, Gottlieb señaló que la agencia intensificará las investigaciones a las casi 600 clínicas de células madre en todo el país, muchas de las cuales ofrecen tratamientos cuya seguridad o efectividad no han sido comprobadas para una amplia gama de enfermedades y lesiones.
En sus fuertes campañas de marketing, estas clínicas ofrecen tratamientos para males ortopédicos, así como para cáncer, lesiones de la columna y condiciones neurológicas tales como el Alzheimer, la demencia, el Parkinson y la ELA. A menudo cobran entre $5,000 y $10,000 por los tratamientos, y persuaden a los pacientes para que regresen para rondas adicionales.
Gottlieb sentenció que ordenó a la agencia “investigar vigorosamente este tipo de clínicas inescrupulosas”. Las acciones de la FDA “también deberían ser una advertencia para todos aquellos que puedan estar causando un daño similar. Tomaremos medidas para asegurar que los estadounidenses no se expongan a riesgos innecesarios”.
La administración Trump declaró su intención de acelerar la aprobación de medicamentos experimentales, y Gottlieb defendió fuertemente la reestructuración al proceso de revisión de la agencia. Pero el lunes señaló que “la FDA no puede permitir que un pequeño número de malos actores se aprovechen de esa promesa para engañar a los pacientes y ponerlos en riesgo”.
Las células madre son aquellas que aún no han asumido una función especializada, tales como convertirse en sangre o músculos, y forman un elemento básico de la creciente oferta de tratamientos de la medicina regenerativa. Los ensayos clínicos han demostrado que algunas terapias con estas células son seguras y eficaces, pero la mayoría de ellas son aún experimentales.
La excitación que rodea el potencial curativo de las células madre ha generado un auge de clínicas que ofrecen tratamientos que no han sido sometidos a rigurosas pruebas.
Si la FDA pone en la mira las clínicas que ofrecen estas terapias estará muy ocupada, aseguró el experto en bioética Leigh Turner, de la Universidad de Minnesota.
El año pasado, Turner y un biólogo celular de UC Davis, Paul Knoepfler, informaron que 351 empresas estadounidenses estaban comercializando tratamientos con células madre en 571 clínicas de todo el país. El sur de California representaba uno de los “puntos críticos” para estos negocios, con 131 clínicas. Pero éstas también florecen en el sur de Florida, Texas, Colorado, Arizona y Nueva York.
Estos centros típicamente comercializan sus servicios directamente a los consumidores, pasando por alto las prácticas médicas establecidas y a los académicos que han planteado dudas sobre la seguridad y la eficacia de los procedimientos. Los tratamientos rara vez están cubiertos por los seguros médicos.
Las clínicas han pasado inadvertidas casi enteramente por la FDA, remarcó Turner. Según él, la carta de la agencia presenta ciertos vacíos que dejan a algunos tratamientos con células madre fuera del alcance de la agencia, pero mientras estas compañías se vuelven más audaces en sus estrategias de marketing y más ambiciosas en su manipulación de las células, es hora de que la FDA ejerza su derecho a exigir evidencia de que los tratamientos son seguros y efectivos, consideró. “Si esta afirmación contundente significa que la FDA planea intensificar la aplicación de la ley -yendo tras los malos actores en el mercado- es algo positivo”, destacó Turner. “Esperemos que sean más que sólo buenas palabras”.
Al referirse a las clínicas que manejan células madre, Gottlieb, quien sobrevivió a un linfoma de Hodgkin, abordó el tema de forma personal. “Conozco muy bien el miedo y la ansiedad que un diagnóstico de cáncer puede tener en un paciente y sus seres queridos, y lo tentador que resulta creer en las afirmaciones audaces -pero vacías- que hacen este tipo de clínicas sin escrúpulos, que venden lo que llaman ‘curas’”, afirmó. “La FDA no permitirá que los actores engañosos se aprovechen de los pacientes vulnerables al pretender tener tratamientos o curaciones para enfermedades graves, sin ninguna prueba de que realmente sean útiles”.
El funcionario resaltó los tratamientos ofrecidos por los California Stem Cell Treatment Centers: “No permitiré especialmente que casos como éste sean pasados por alto. Tenemos buenas razones médicas para creer que estos supuestos procedimientos pueden realmente dañar a los pacientes y empeorar sus condiciones”.
Knoepfler resaltó que las acciones del lunes fueron “una gran cosa”. “No estaba seguro, especialmente en el marco del gobierno de Trump, de que esto ocurriría”, manifestó. “Pero me sorprendí gratamente: fueron palabras y acciones, y las palabras fueron bastante directas”.
Traducción: Valeria Agis
Para leer esta nota en inglés, haga clic aquí
Suscríbase al Kiosco Digital
Encuentre noticias sobre su comunidad, entretenimiento, eventos locales y todo lo que desea saber del mundo del deporte y de sus equipos preferidos.
Ocasionalmente, puede recibir contenido promocional del Los Angeles Times en Español.



